|
单选题 某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和H2(g)五种物质,并建立了下述平衡: H2O(g) + C(s) = H2(g) + CO(g)、CO2(g) + H2(g) = H2O(g) + CO(g)、CO2(g) + C(s) = 2 CO(g)则该系统的组分数K为 A: 3 B: 2 C: 1 D: 4 单选题 有四种浓度均为0.01 mol・kg-1的电解质溶液,其中平均活度系数最大的是 A: KCl B: CaCl2 C: Na2SO4 D: AlCl3 单选题 有关基元反应描述不正确是 A: 基元反应的级数一定是整数 B: 基元反应的级数与反应分子数相等 C: 基元反应进行时无中间产物 D: 基元反应不一定符合质量定律 单选题 理想溶液的通性是 A: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合<0 B: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合=0 C: ΔV混合>0 ΔH混合>0 ΔS混合>0 ΔG混合<0 D: ΔV混合=0 ΔH混合=0 ΔS混合=0 ΔG混合=0 单选题 2MgO(s)+2Cl2(g)→2MgCl2(s)+O2(g)达平衡后,增加总压(气体按理想气体考虑),则 A: n(O2)增加、n(Cl2)减少、Kθ增大 B: n(O2)减小、n(Cl2)减少、Kθ减小 C: n(O2)增加、n(Cl2)减少、Kθ不变 D: n(O2)减小、n(Cl2)增大、Kθ不变 单选题 理想液态混合物中任一组分B,其偏摩尔量与摩尔量的关系为 A: HB,m= 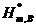 B: VB,m≠  C: GB,m= 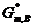 D: SB,m= 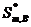 单选题 对于单组分系统的气液平衡,当lnp与T呈线性关系时,则汽化过程 A: ΔVH=0 B: ΔVH=常数 C: ΔVS=0 D: ΔVH=f(T) 单选题 1mol单原子理想气体,在300K时绝热压缩到500K,其ΔH=( )J A: 2494 B: 4157 C: 5000 D: 5820 单选题 已知1000K时,CO(g)+0.5O2(g)→CO2(g)的=1.659×1010及C(s)+ CO2(g) →2CO(g)的=1.719,则反应C(s)+ 0.5O2(g) →CO(g)的为 A: 9.651×109 B: 1.036×10-10 C: 2.852×1010 D: 4.731×1020 单选题 已知298K时,反应H2(g)+Cl2(g)→2HCl(g)的ΔrH=-185kJ,则此反应的ΔrU A: 无法知道 B: 大于ΔrH C: 小于ΔrH D: 等于ΔrH 单选题 298K时,反应C6H6(l)+7.5O2(g)→3H2O(l)+6CO2(g)的ΔrH-ΔrU约为 A: -3.7kJ B: 1.2kJ C: -1.2kJ D: 3.7kJ 单选题 在300K及pθ下,水的化学势μl与水汽的化学势μg的关系是 A: μl=μg B: μl>μg C: μl<μg D: 不确定 单选题 反应N2(g)+3H2(g)→2NH3(g)已达平衡,在保持温度、压力不变的条件下,往系统中加入惰性气体后,则 A: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ不变 B: p(N2)减小、n(H2)减少、p(NH3)增大、Kθ不变 C: p(N2)、p(H2)、p(NH3)均减小,Kθ不变 D: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ减小 单选题 在300K时,5mol的理想气体由1dm3等温膨胀到10dm3,则过程的ΔS等于 A: 11.51R B: -11.51R C: 2.303R D: -2.303R 单选题 水煤气发生炉中能发生的反应有:(1)CO2(g)+C(s)→2CO(g),(2)H2O(g)+C(s)→H2(g)+CO(g),(3)CO2(g)+H2(g)→H2O(g)+CO(g) 。当体系达到平衡后,有 A: K=2,f=2 B: K=3,f=3 C: K=3,f=4 D: K=2,f=3 判断 只需用热力第二定律就可以解决化学变化与相变化的方向和限度问题。 判断 亥姆霍兹能与吉布斯能都是能量的表现形式 判断 若一个化学反应的△rH与温度无关,其△rS也与温度无关 判断 电池放电时,溶液中带负电荷的离子向阴极迁移 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 对于反应前后分子数相等的化学变化,系统压力的改变对平衡没有影响。 判断 时间是热力学的一个重要参量 判断 一定温度压力下,对于△rGm>0的反应,需要选用合适的催化剂才能使其自发进行。 判断 当反应条件改变时,同一化学反应表现出不同的反应级数,就意味着其反应机理也发生了改变 判断 在单相区相点与物系点是重合的 单选题 热力学第一定律的数学表达式ΔU = Q+W 只能适用于 A: 理想气体 B: 封闭体系 C: 实际气体 D: 敞开体系 单选题 在300K时,5mol的理想气体由1dm3等温膨胀到10dm3,则过程的ΔS等于 A: 11.51R B: -11.51R C: 2.303R D: -2.303R 单选题 某非缔合性液体在正常沸点时汽化热为22000J・mol-1,则其正常沸点最接近 A: 500℃ B: 500K C: 250K D: 100℃ 单选题 根据某一反应的△rGmθ值,不能确定的是 A: 标准状态下自发变化的方向 B: 在△rGmθ所对应的温度下的平衡位置 C: 在标准状态下系统所能做的最大非体积功 D: 提高温度与反应速率的变化趋势 单选题 TK时,1mol理想气体的绝热可逆膨胀过程 A: ΔS<0 B: ΔS>0 C: ΔS=0 D: 不确定 单选题 当10molN2 (g)与30molH2 (g)混合,生成6molNH3(g),若以下式:N2(g) +3H2(g) →2NH3(g) 表示反应关系。则反应进度为: A: 1mol B: 2mol C: 3mol D: 6mol 单选题 某一反应在一定条件下的平衡转化率为25.3%,当有催化剂存在时,其平衡转化率是 A: 大于25.3% B: 小于25.3% C: 等于25.3% D: 不确定 单选题 已知气相反应2NO(g)+O2(g)→2NO2(g)是放热反应,当反应达到平衡时,可采用哪组方法使平衡向右移动 A: 降温和减压 B: 升温和增压 C: 升温和减压 D: 降温和增压 单选题 同一温度下,同一气体物质的Cp,m与CV,m之间有 A: CP,m<CV,m B: CP,m>CV,m C: CP,m=CV,m D: 无法比较 单选题 在100kPa下,I2在液态水及CCl4中达到分配平衡(无固态碘存在),则该系统的 A: f* =1 B: f* =2 C: f* =0 D: f* =3 单选题 A: -Q/T B: -5Q/T C: Q/5T D: 5Q/T 单选题 某化学反应的△rHmθ<0,△rSmθ>0,则反应的 A: Kθ>1且随温度升高而增大 B: Kθ<1且随温度升高而减小 C: Kθ<1且随温度升高而增大 D: Kθ>1且随温度升高而减小 单选题 反应2C(s)+O2(g)→2CO(g) △rGmθ=-232600-167.8T(J/mol),当温度增加时 A: △rGmθ变负,反应更完全 B: Kθ变大,反应更完全 C: Kθ变大,反应更不完全 D: Kθ变小,反应更不完全 单选题 在298K时反应CuSO4・3H2O(s) →CuSO4(s)+3H2O(g)的Kθ为10-6,则平衡的水蒸气分压为 A: 10-6 pθ B: 10-2 pθ C: 10-3 pθ D: 10-4 pθ 单选题 若隔离系统中发生具有确定方向的变化,则系统的熵 A: 保持不变 B: 总是减小 C: 总是增大 D: 可任意变化 判断 对于反应前后分子数相等的气相化学变化,系统压力的改变对平衡没有影响。 判断 焓是热的一种能量表现形式 判断 一定温度下化学反应的平衡常数是一个定值,但与化学反应方程式的书写方式有关 判断 一定温度压力下,对于△rGm>0的反应,需要选用合适的催化剂才能使其自发进行。 判断 偏摩尔热力学能也是化学势的定义之一 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 对于反应前后分子数相等的化学变化,系统压力的改变对平衡没有影响。 判断 热力学第一定律主要来研究和解决化学变化以及相变化中的热效应问题 判断 在温度、浓度和电场梯度都相同的情形下,氯化氢、氯化钾、氯化钠三种溶液中氯离子的迁移数是相同的 判断 在稀溶液范围内,随电解质溶液浓度的增大,离子强度增大,平均活度系数随之减小 单选题 某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和H2(g)五种物质,并建立了下述平衡: H2O(g) + C(s) = H2(g) + CO(g)、CO2(g) + H2(g) = H2O(g) + CO(g)、CO2(g) + C(s) = 2 CO(g)则该系统的组分数K为 A: 3 B: 2 C: 1 D: 4 单选题 有四种浓度均为0.01 mol・kg-1的电解质溶液,其中平均活度系数最大的是 A: KCl B: CaCl2 C: Na2SO4 D: AlCl3 单选题 有关基元反应描述不正确是 A: 基元反应的级数一定是整数 B: 基元反应的级数与反应分子数相等 C: 基元反应进行时无中间产物 D: 基元反应不一定符合质量定律 单选题 理想溶液的通性是 A: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合<0 B: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合=0 C: ΔV混合>0 ΔH混合>0 ΔS混合>0 ΔG混合<0 D: ΔV混合=0 ΔH混合=0 ΔS混合=0 ΔG混合=0 单选题 2MgO(s)+2Cl2(g)→2MgCl2(s)+O2(g)达平衡后,增加总压(气体按理想气体考虑),则 A: n(O2)增加、n(Cl2)减少、Kθ增大 B: n(O2)减小、n(Cl2)减少、Kθ减小 C: n(O2)增加、n(Cl2)减少、Kθ不变 D: n(O2)减小、n(Cl2)增大、Kθ不变 单选题 理想液态混合物中任一组分B,其偏摩尔量与摩尔量的关系为 A: HB,m= 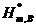 B: VB,m≠  C: GB,m= 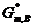 D: SB,m= 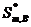 单选题 对于单组分系统的气液平衡,当lnp与T呈线性关系时,则汽化过程 A: ΔVH=0 B: ΔVH=常数 C: ΔVS=0 D: ΔVH=f(T) 单选题 1mol单原子理想气体,在300K时绝热压缩到500K,其ΔH=( )J A: 2494 B: 4157 C: 5000 D: 5820 单选题 已知1000K时,CO(g)+0.5O2(g)→CO2(g)的=1.659×1010及C(s)+ CO2(g) →2CO(g)的=1.719,则反应C(s)+ 0.5O2(g) →CO(g)的为 A: 9.651×109 B: 1.036×10-10 C: 2.852×1010 D: 4.731×1020 单选题 已知298K时,反应H2(g)+Cl2(g)→2HCl(g)的ΔrH=-185kJ,则此反应的ΔrU A: 无法知道 B: 大于ΔrH C: 小于ΔrH D: 等于ΔrH 单选题 298K时,反应C6H6(l)+7.5O2(g)→3H2O(l)+6CO2(g)的ΔrH-ΔrU约为 A: -3.7kJ B: 1.2kJ C: -1.2kJ D: 3.7kJ 单选题 在300K及pθ下,水的化学势μl与水汽的化学势μg的关系是 A: μl=μg B: μl>μg C: μl<μg D: 不确定 单选题 反应N2(g)+3H2(g)→2NH3(g)已达平衡,在保持温度、压力不变的条件下,往系统中加入惰性气体后,则 A: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ不变 B: p(N2)减小、n(H2)减少、p(NH3)增大、Kθ不变 C: p(N2)、p(H2)、p(NH3)均减小,Kθ不变 D: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ减小 单选题 在300K时,5mol的理想气体由1dm3等温膨胀到10dm3,则过程的ΔS等于 A: 11.51R B: -11.51R C: 2.303R D: -2.303R 单选题 水煤气发生炉中能发生的反应有:(1)CO2(g)+C(s)→2CO(g),(2)H2O(g)+C(s)→H2(g)+CO(g),(3)CO2(g)+H2(g)→H2O(g)+CO(g) 。当体系达到平衡后,有 A: K=2,f=2 B: K=3,f=3 C: K=3,f=4 D: K=2,f=3 判断 只需用热力第二定律就可以解决化学变化与相变化的方向和限度问题。 判断 亥姆霍兹能与吉布斯能都是能量的表现形式 判断 若一个化学反应的△rH与温度无关,其△rS也与温度无关 判断 电池放电时,溶液中带负电荷的离子向阴极迁移 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 对于反应前后分子数相等的化学变化,系统压力的改变对平衡没有影响。 判断 时间是热力学的一个重要参量 判断 一定温度压力下,对于△rGm>0的反应,需要选用合适的催化剂才能使其自发进行。 判断 当反应条件改变时,同一化学反应表现出不同的反应级数,就意味着其反应机理也发生了改变 判断 在单相区相点与物系点是重合的 单选题 若电池反应所对应的电池电动势为负值,表示此电池反应是 A: 正向进行 B: 逆向进行 C: 不能进行 D: 方向不确定 单选题 化学反应 CO(g) + 2H2(g) = CH3OH(g)的△rGmθ与温度T的关系为:△rGmθ= -21660 + 52.92T,若要使反应的平衡常数Kθ>1,则应控制的反应温度为: A: 必须低于409.3℃ B: 必须高于409.3K C: 必须低于409.3K D: 必须等于409.3K 单选题 已知某理想气体的,则该气体为 A: 单原子 B: 双原子 C: 三原子 D: 四原子 单选题 在以热力学能表示的化学势定义中,与下列哪两个条件保持不变有关 A: (S,V) B: (S,p) C: (T,V) D: (T,p) 单选题 反应N2(g)+3H2(g)→2NH3(g)已达平衡,在保持温度、压力不变的条件下,往系统中加入惰性气体后,则 A: n(N2)减小、n(H2)减少、n(NH3)增大、Kθ不变 B: n(N2)减小、n(H2)减少、n(NH3)增大、Kθ增大 C: n(N2)、n(H2)、n(NH3)不变,Kθ不变 D: n(N2)增大、n(H2)增大、n(NH3)减小、Kθ不变 单选题 0℃及pθ下,1mol水结冰时,系统的熵变 A: ΔS<0 B: ΔS>0 C: ΔS=0 D: 不确定 单选题 NH4HS(s)和任意量的NH3(g)及H2S(g)达到化学平衡时,有 A: K =2,Φ= 2,f =2 B: K =1,Φ= 2,f =1 C: K =2,Φ= 3,f =2 D: K =3,Φ= 2,f =3 单选题 使一过程的ΔS=0应满足的条件是 A: 绝热可逆过程 B: 等容绝热过程 C: 绝热过程 D: 等压绝热过程 单选题 298K,当H2SO4溶液的浓度从0.01mol・kg-1增加到0.1 mol・kg-1时,其电导率κ和Λm将 A: κ减小,Λm增加 B: κ增加,Λm增加 C: κ减小,Λm减小 D: κ增加,Λm减小 单选题 在克劳修斯-克拉佩龙中 A: ΔH与ΔV的正负符号必定是相同的 B: ΔH与ΔV的正负符号必定是相反的 C: ΔH与ΔV的正负符号必定是无关的 D: ΔH与ΔV的数值必定是相等的 单选题 理想气体在等温条件下反抗恒定外压膨胀,系统的熵变 A: ΔS<0 B: ΔS>0 C: ΔS=0 D: 不确定 单选题 特鲁顿规则适用于 A: 任何纯液体 B: 二元溶液 C: 缔合性液体 D: 正常液体 单选题 已知温度T时反应H2O(g) →H2(g)+O2(g)的及反应CO2(g) →CO(g)+O2(g)的则同温度下反应CO(g)+H2O(g) →CO2(g)+H2(g)的等于 A: 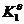 + +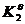 B: 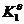 ・ ・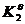 C: 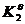 / /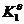 D: 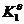 / / 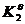 单选题 N2与O2混合气体的绝热可逆压缩过程中,系统的热力学函数变化值为零的是 A: U B: H C: S D: G 单选题 已知气相反应2NO(g)+O2(g)→2NO2(g)是放热反应,当反应达到平衡时,可采用哪组方法使平衡向右移动 A: 降温和减压 B: 升温和增压 C: 升温和减压 D: 降温和增压 判断 硫氢化铵在真空容器中分解与在充有一定氨气的容器中分解,其独立组分数是一样的 判断 时间是热力学的一个重要参量 判断 一定温度下化学反应的平衡常数是一个定值,但与化学反应方程式的书写方式有关 判断 恒沸点与纯物质沸点的性质是完全一样的 判断 根据dG=-SdT+Vdp,任意等温等压过程系统的dG都会为零 判断 热力学第一定律主要来研究和解决化学变化以及相变化中的热效应问题 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 在温度、浓度和电场梯度都相同的情形下,氯化氢、氯化钾、氯化钠三种溶液中氯离子的迁移数是相同的 判断 从相同的始态出发,绝热可逆过程与绝热不可逆过程不可能到达相同的终态 判断 不做功的封闭系统未必就是孤立系统 单选题 某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和H2(g)五种物质,并建立了下述平衡: H2O(g) + C(s) = H2(g) + CO(g)、CO2(g) + H2(g) = H2O(g) + CO(g)、CO2(g) + C(s) = 2 CO(g)则该系统的组分数K为 A: 3 B: 2 C: 1 D: 4 单选题 有四种浓度均为0.01 mol・kg-1的电解质溶液,其中平均活度系数最大的是 A: KCl B: CaCl2 C: Na2SO4 D: AlCl3 单选题 有关基元反应描述不正确是 A: 基元反应的级数一定是整数 B: 基元反应的级数与反应分子数相等 C: 基元反应进行时无中间产物 D: 基元反应不一定符合质量定律 单选题 理想溶液的通性是 A: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合<0 B: ΔV混合=0 ΔH混合=0 ΔS混合>0 ΔG混合=0 C: ΔV混合>0 ΔH混合>0 ΔS混合>0 ΔG混合<0 D: ΔV混合=0 ΔH混合=0 ΔS混合=0 ΔG混合=0 单选题 2MgO(s)+2Cl2(g)→2MgCl2(s)+O2(g)达平衡后,增加总压(气体按理想气体考虑),则 A: n(O2)增加、n(Cl2)减少、Kθ增大 B: n(O2)减小、n(Cl2)减少、Kθ减小 C: n(O2)增加、n(Cl2)减少、Kθ不变 D: n(O2)减小、n(Cl2)增大、Kθ不变 单选题 理想液态混合物中任一组分B,其偏摩尔量与摩尔量的关系为 A: HB,m= 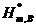 B: VB,m≠  C: GB,m= 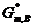 D: SB,m= 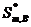 单选题 对于单组分系统的气液平衡,当lnp与T呈线性关系时,则汽化过程 A: ΔVH=0 B: ΔVH=常数 C: ΔVS=0 D: ΔVH=f(T) 单选题 1mol单原子理想气体,在300K时绝热压缩到500K,其ΔH=( )J A: 2494 B: 4157 C: 5000 D: 5820 单选题 已知1000K时,CO(g)+0.5O2(g)→CO2(g)的=1.659×1010及C(s)+ CO2(g) →2CO(g)的=1.719,则反应C(s)+ 0.5O2(g) →CO(g)的为 A: 9.651×109 B: 1.036×10-10 C: 2.852×1010 D: 4.731×1020 单选题 已知298K时,反应H2(g)+Cl2(g)→2HCl(g)的ΔrH=-185kJ,则此反应的ΔrU A: 无法知道 B: 大于ΔrH C: 小于ΔrH D: 等于ΔrH 单选题 298K时,反应C6H6(l)+7.5O2(g)→3H2O(l)+6CO2(g)的ΔrH-ΔrU约为 A: -3.7kJ B: 1.2kJ C: -1.2kJ D: 3.7kJ 单选题 在300K及pθ下,水的化学势μl与水汽的化学势μg的关系是 A: μl=μg B: μl>μg C: μl<μg D: 不确定 单选题 反应N2(g)+3H2(g)→2NH3(g)已达平衡,在保持温度、压力不变的条件下,往系统中加入惰性气体后,则 A: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ不变 B: p(N2)减小、n(H2)减少、p(NH3)增大、Kθ不变 C: p(N2)、p(H2)、p(NH3)均减小,Kθ不变 D: p(N2)增大、p(H2)增大、p(NH3)减小、Kθ减小 单选题 在300K时,5mol的理想气体由1dm3等温膨胀到10dm3,则过程的ΔS等于 A: 11.51R B: -11.51R C: 2.303R D: -2.303R 单选题 水煤气发生炉中能发生的反应有:(1)CO2(g)+C(s)→2CO(g),(2)H2O(g)+C(s)→H2(g)+CO(g),(3)CO2(g)+H2(g)→H2O(g)+CO(g) 。当体系达到平衡后,有 A: K=2,f=2 B: K=3,f=3 C: K=3,f=4 D: K=2,f=3 判断 只需用热力第二定律就可以解决化学变化与相变化的方向和限度问题。 判断 亥姆霍兹能与吉布斯能都是能量的表现形式 判断 若一个化学反应的△rH与温度无关,其△rS也与温度无关 判断 电池放电时,溶液中带负电荷的离子向阴极迁移 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 对于反应前后分子数相等的化学变化,系统压力的改变对平衡没有影响。 判断 时间是热力学的一个重要参量 判断 一定温度压力下,对于△rGm>0的反应,需要选用合适的催化剂才能使其自发进行。 判断 当反应条件改变时,同一化学反应表现出不同的反应级数,就意味着其反应机理也发生了改变 判断 在单相区相点与物系点是重合的 单选题 若电池反应所对应的电池电动势为负值,表示此电池反应是 A: 正向进行 B: 逆向进行 C: 不能进行 D: 方向不确定 单选题 化学反应 CO(g) + 2H2(g) = CH3OH(g)的△rGmθ与温度T的关系为:△rGmθ= -21660 + 52.92T,若要使反应的平衡常数Kθ>1,则应控制的反应温度为: A: 必须低于409.3℃ B: 必须高于409.3K C: 必须低于409.3K D: 必须等于409.3K 单选题 已知某理想气体的,则该气体为 A: 单原子 B: 双原子 C: 三原子 D: 四原子 单选题 在以热力学能表示的化学势定义中,与下列哪两个条件保持不变有关 A: (S,V) B: (S,p) C: (T,V) D: (T,p) 单选题 反应N2(g)+3H2(g)→2NH3(g)已达平衡,在保持温度、压力不变的条件下,往系统中加入惰性气体后,则 A: n(N2)减小、n(H2)减少、n(NH3)增大、Kθ不变 B: n(N2)减小、n(H2)减少、n(NH3)增大、Kθ增大 C: n(N2)、n(H2)、n(NH3)不变,Kθ不变 D: n(N2)增大、n(H2)增大、n(NH3)减小、Kθ不变 单选题 0℃及pθ下,1mol水结冰时,系统的熵变 A: ΔS<0 B: ΔS>0 C: ΔS=0 D: 不确定 单选题 NH4HS(s)和任意量的NH3(g)及H2S(g)达到化学平衡时,有 A: K =2,Φ= 2,f =2 B: K =1,Φ= 2,f =1 C: K =2,Φ= 3,f =2 D: K =3,Φ= 2,f =3 单选题 使一过程的ΔS=0应满足的条件是 A: 绝热可逆过程 B: 等容绝热过程 C: 绝热过程 D: 等压绝热过程 单选题 298K,当H2SO4溶液的浓度从0.01mol・kg-1增加到0.1 mol・kg-1时,其电导率κ和Λm将 A: κ减小,Λm增加 B: κ增加,Λm增加 C: κ减小,Λm减小 D: κ增加,Λm减小 单选题 在克劳修斯-克拉佩龙中 A: ΔH与ΔV的正负符号必定是相同的 B: ΔH与ΔV的正负符号必定是相反的 C: ΔH与ΔV的正负符号必定是无关的 D: ΔH与ΔV的数值必定是相等的 单选题 理想气体在等温条件下反抗恒定外压膨胀,系统的熵变 A: ΔS<0 B: ΔS>0 C: ΔS=0 D: 不确定 单选题 特鲁顿规则适用于 A: 任何纯液体 B: 二元溶液 C: 缔合性液体 D: 正常液体 单选题 已知温度T时反应H2O(g) →H2(g)+O2(g)的及反应CO2(g) →CO(g)+O2(g)的则同温度下反应CO(g)+H2O(g) →CO2(g)+H2(g)的等于 A: 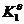 + +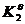 B: 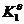 ・ ・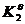 C: 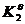 / /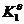 D: 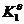 / /  单选题 N2与O2混合气体的绝热可逆压缩过程中,系统的热力学函数变化值为零的是 A: U B: H C: S D: G 单选题 已知气相反应2NO(g)+O2(g)→2NO2(g)是放热反应,当反应达到平衡时,可采用哪组方法使平衡向右移动 A: 降温和减压 B: 升温和增压 C: 升温和减压 D: 降温和增压 判断 硫氢化铵在真空容器中分解与在充有一定氨气的容器中分解,其独立组分数是一样的 判断 时间是热力学的一个重要参量 判断 一定温度下化学反应的平衡常数是一个定值,但与化学反应方程式的书写方式有关 判断 恒沸点与纯物质沸点的性质是完全一样的 判断 根据dG=-SdT+Vdp,任意等温等压过程系统的dG都会为零 判断 热力学第一定律主要来研究和解决化学变化以及相变化中的热效应问题 判断 在等温等压下化学反应的反应热总是等于△rH,所以△rS总是等于△rH/△rS 判断 在温度、浓度和电场梯度都相同的情形下,氯化氢、氯化钾、氯化钠三种溶液中氯离子的迁移数是相同的 判断 从相同的始态出发,绝热可逆过程与绝热不可逆过程不可能到达相同的终态 判断 不做功的封闭系统未必就是孤立系统 (责任编辑:admin)要这答案加QQ:800020900 或加微信:q800020900 获取 |

